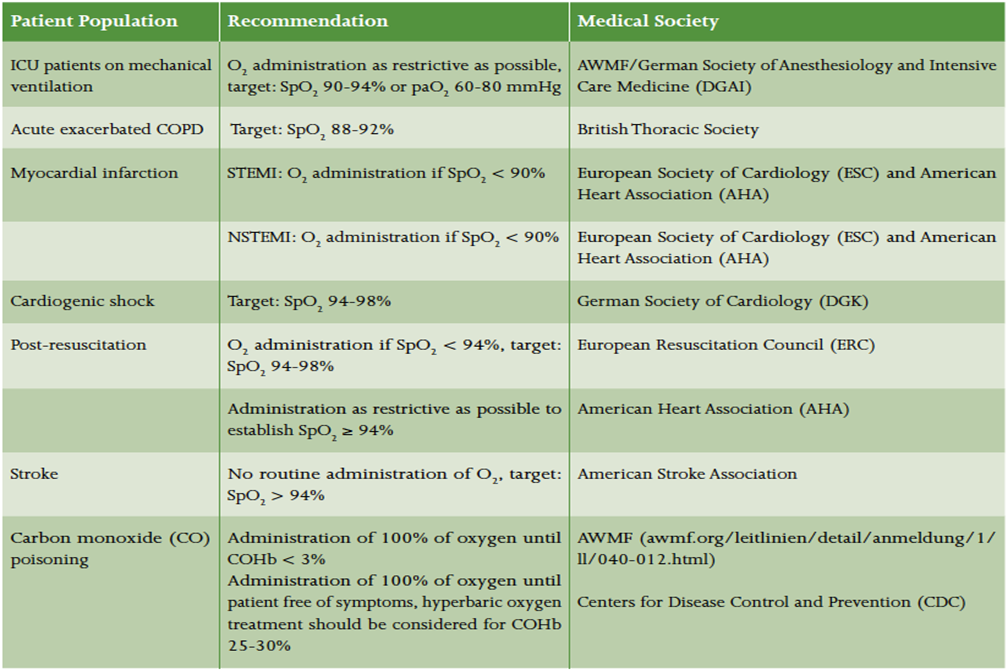
全面系统的了解重症监护治疗中的氧疗
时间:2021-10-25 17:01:53 热度:37.1℃ 作者:网络
氧疗被广泛用于重症监护和急诊医学,是维持有氧代谢所必需。尽管氧疗可以挽救生命,但也有研究表明不加区分地给氧可能会增加发病率和死亡率,这可能是由于高氧分压促进了活性氧的生成。对于最佳氧疗值的探索仍在继续,未来可能阐明用氧的量-效关系,也需要进一步明确不同条件下的最佳氧疗目标;由于高氧至少不会获益,甚至带来损伤,然而我们也必须避免低氧血症,故目标性给氧策略非常重要。

简要回顾
1771年:Carl Wilhelm Scheele & Joseph Priestley 发现氧气
1783年:氧气用于结核病和新生儿窒息治疗
1889年:J. H. Draeger 应用氧气阀门
1902年:C. von Linde 升级了制氧工艺
1912年:Bornsein 记录人吸入高氧后不良反应
现在对氧的认识现在,我们对氧的认识已经明显加深了,不只限于观察到氧的毒性作用。
血液中氧气主要由血红蛋白运输,依据S形氧解离曲线,很少量的氧在80 mmHg以上结合Hb输送,常压下物理溶解氧是微不足道的。
氧气参与呼吸链,在细胞色素氧化酶作用下帮助形成质子跨膜动作电位梯度,这是合成ATP所必须的。
如果氧气不足,呼吸链将会受到影响,能量的产生只限于无氧糖酵解。
临床上,低氧导致乳酸酸中毒和中枢神经系统等对氧气敏感的组织的坏死,因此,氧气对于人类是很重要的,在存在低氧血症的急诊情况下,氧气的应用是可以挽救生命的。
然而,有时候我们忘记了之前医学研究中指出的被称为“氧中毒”的不良反应。尽管我们知道过多的氧会导致活性氧的产生,进而造成细胞损伤,使细胞凋亡和坏死,但我们还是经常能看到重症患者血气分析中的氧分压远高于正常值。其他因素如感染状态下释放的PAMPs,进一步加剧细胞损伤。细胞凋亡或坏死后释放其他介质和DAMPs,它们与活性氧共同导致进一步的细胞损伤,形成恶性循环。高氧分压促进了活性氧的生成。 ROS等对细胞损伤的恶性循环
 Helmerhorst HJ, Schultz MJ, van der Voort PH et al. (2015) Bench-to-bedside review: the effects of hyperoxia during critical illness. Crit Care, 19(284):015-0996.
高氧和临床的关系
在心肌梗死或缺血性卒中这一类血管阻塞性疾病中,初看提升氧分压试图使缺血的组织增加氧合是符合逻辑的,但相反,这有可能使缺血组织通过上述恶性循环而死亡,由现有的数据来看,后者是主要的。
AVOID研究
急性ST段抬高型心肌梗死患者
Helmerhorst HJ, Schultz MJ, van der Voort PH et al. (2015) Bench-to-bedside review: the effects of hyperoxia during critical illness. Crit Care, 19(284):015-0996.
高氧和临床的关系
在心肌梗死或缺血性卒中这一类血管阻塞性疾病中,初看提升氧分压试图使缺血的组织增加氧合是符合逻辑的,但相反,这有可能使缺血组织通过上述恶性循环而死亡,由现有的数据来看,后者是主要的。
AVOID研究
急性ST段抬高型心肌梗死患者
|
干预组:面罩吸氧8 L/min。 对照组:不常规给氧(如SpO2<94%,鼻导管4 L/min或面罩8 L/min使SpO2>94%)。 终点:72 h内定时检测血cTnI、CK等指标。6个月后行心脏核磁检查心肌坏死情况。 结果:干预组CK和6个月后心脏核磁情况较对照组差。 另外,干预组再梗死率和心律失常发生率更高。 |
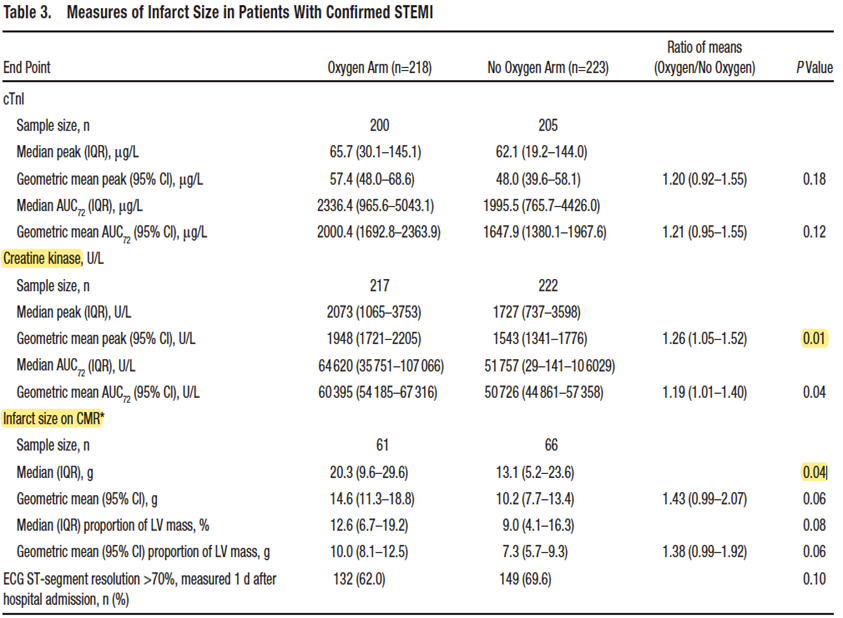
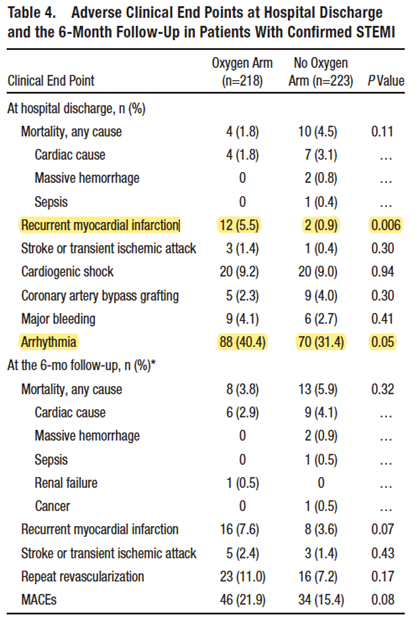
Stub D, Smith K, Bernard S, et al. Air Versus Oxygen in ST-Segment-Elevation Myocardial Infarction[J]. Circulation, 2015,131(24):2143-2150.
DETO2X-AMI 研究 急性心肌梗死患者,基础SpO2≥90%且未吸氧|
干预组:6 L/min ,6~12 h 对照组:室内空气 SpO2<90%给氧 主要终点:1年内死亡率 次要终点:30 d死亡率,再梗死入院率、房颤率、心源性休克发生率 试验结果:主要终点及次要终点均无差异 |
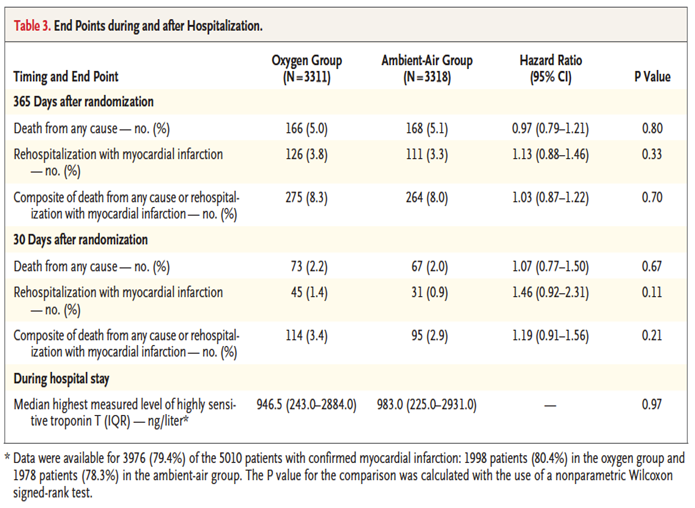

Hofmann R, James S K, Jernberg T, et al. Oxygen Therapy in Suspected Acute Myocardial Infarction[J]. N Engl J Med, 2017, 377(13):1240-1249.
| 综合上述两项研究,心梗患者,给氧可能有害,至少无益。 正如现在欧洲和美国指南建议SPO2≥90%,不给氧。 |

氧气有收缩血管的作用,其机制可能是抑制NO。没有冠心病的患者乙酰胆碱激发试验同时吸入纯氧导致冠脉痉挛,乙酰胆碱激发试验同时吸入空气则没有发生痉挛。

McNulty P H, King N, Scott S, et al. Effects of supplemental oxygen administration on coronary blood flow in patients undergoing cardiac catheterization[J]. Am J Physiol Heart Circ Physiol, 2005, 288.
SO2S研究 关于缺血性卒中,SO2S研究对8000余不存在低氧血症的急性卒中患者。|
干预组1:持续给氧(72 h)。 干预组2:仅在夜间给氧(21:00-07:00,3n)。 对照组:不常规给氧。 *基础SpO2≤93%,3 L/min,基础SpO2>93%,2 L/min,每组SpO2都在94%以上。 观察终点:90天mRC。 结果:各组modified Rankin scale无差异。 该研究被纳入指南,SpO2 94%~98%。 |

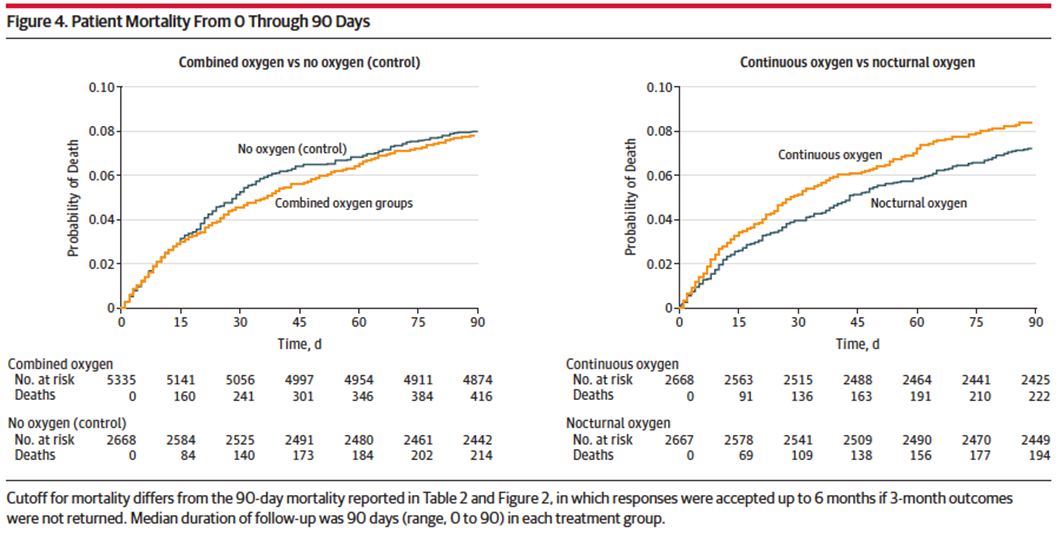 在非缺氧的急性卒中患者中,预防性地使用低剂量的氧气补充并不能减少3个月的死亡或残疾。这些发现并不支持在这种情况下使用低剂量氧。
在非缺氧的急性卒中患者中,预防性地使用低剂量的氧气补充并不能减少3个月的死亡或残疾。这些发现并不支持在这种情况下使用低剂量氧。
Roffe C, Nevatte T, Sim J, et al. Effect of Routine Low-Dose Oxygen Supplementation on Death and Disability in Adults With Acute Stroke: The Stroke Oxygen Study Randomized Clinical Trial[J]. JAMA, 2017,318(12):1125-1135.

一项重症机械通气的患者回顾分析,氧分压和病死率关系呈U形曲线。PaO2 65~80 mmHg生存率最高。这一限值和人们能接受的严格的理论值相符:
*氧分压<60 mmHg,SpO2将降至90%以下,这时缺氧的风险将增加;
*氧分压>80 mmHg,即使每增加一点儿氧气,也会增加活性氧的产生。
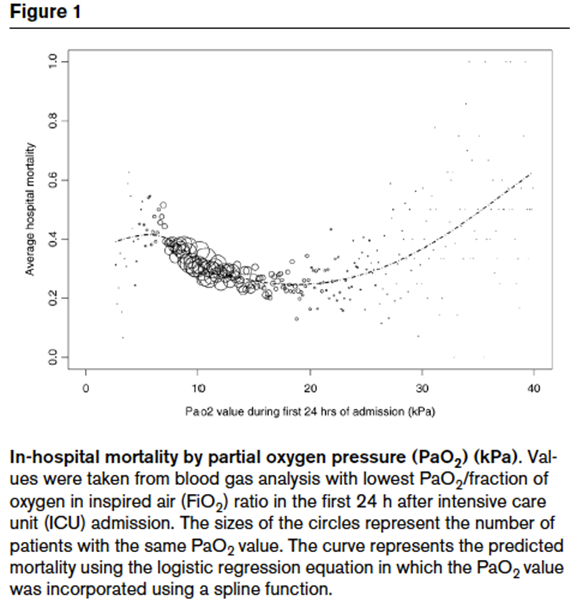
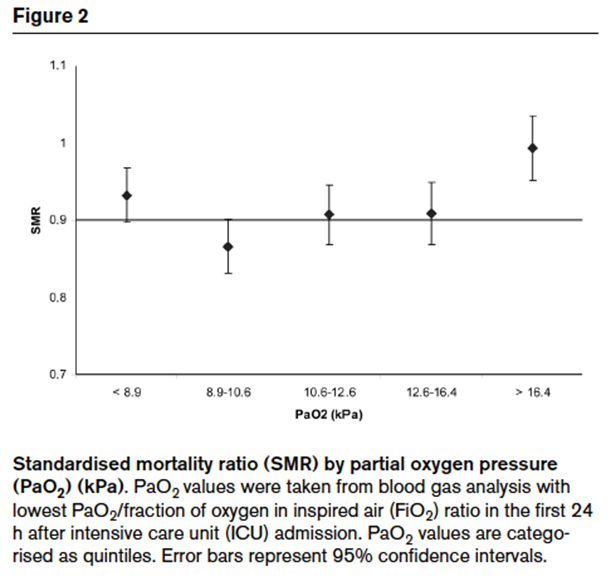
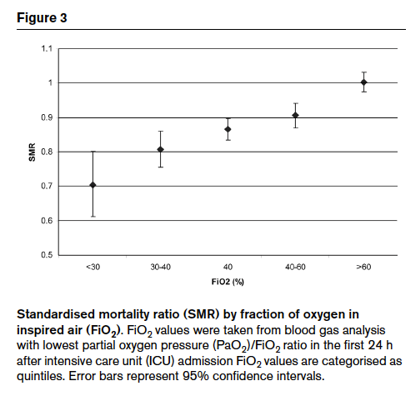
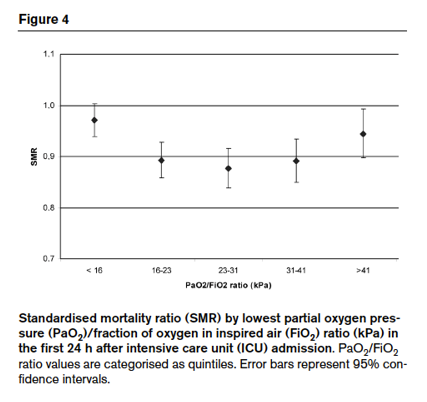
de Jonge E, Peelen L, Keijzers PJ, et al. Association between administered oxygen, arterial partial oxygen pressure and mortality in mechanically ventilated intensive care unit patients. Crit Care, 2008,12(6):1-8.
OXYGEN-ICU研究
单中心研究 Medical 77:86 , Surgical 139:132
| 干预组:氧浓度最低40% → PaO2 150 mmHg,SpO2 97%~100%。(median PaO2102 mmHg [IQR,88~116])。 对照组:最低氧浓度 → PaO2 70~100 mmHg,SpO2 94%~98%。(median PaO2 87 mmHg [IQR, 79~97])。 主要终点:ICU死亡率。 次要终点:入ICU 48 h或以后新发器官功能衰竭。 结果:干预组死亡率、休克、肝衰竭、菌血症等高于对照组。 |
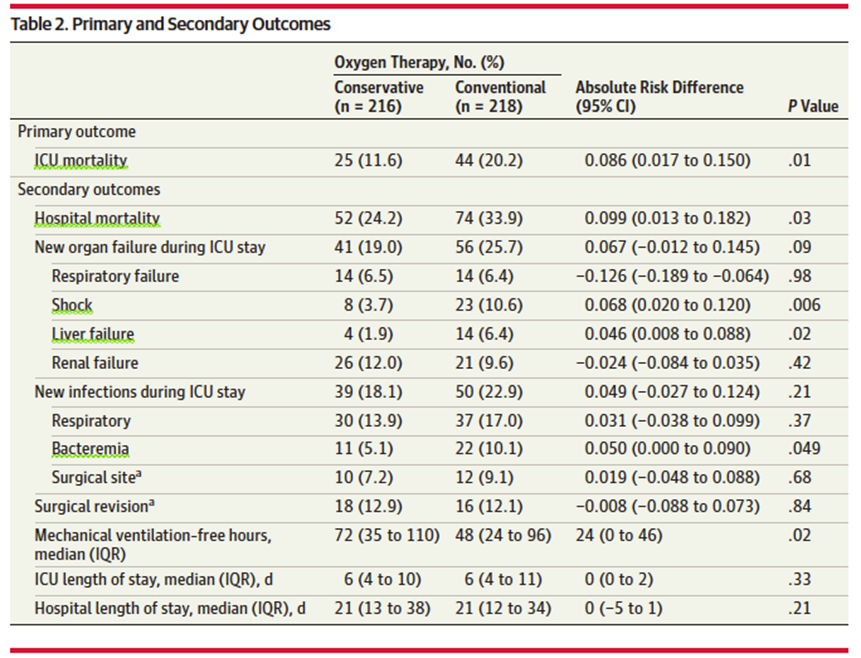
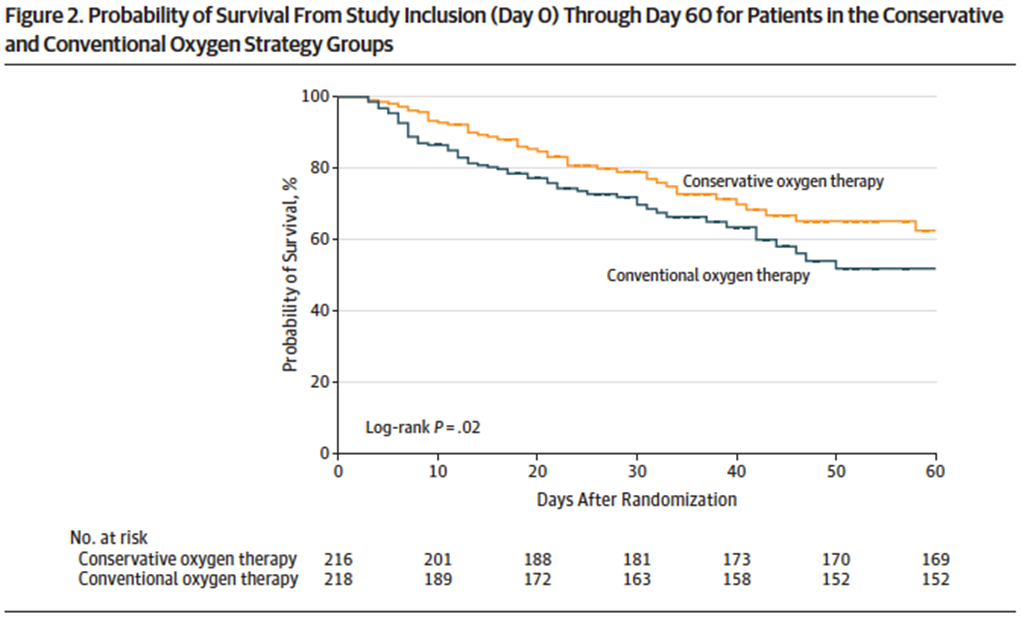
Girardis M, Busani S, Damiani E, et al. Effect of Conservative vs Conventional Oxygen Therapy on Mortality Among Patients in an Intensive Care Unit: The Oxygen-ICU Randomized Clinical Trial[J]. JAMA, 2016, 316(15):1583-1589.
HYPER2S 研究 ICU接受机械通气的脓毒症患者
| 干预组:FiO2 100% (24 h) 。 对照组:FiO2→SpO2 88%~95%(24 h)。 主要终点事件:28 d死亡率。 次要终点事件:90 d死亡率,前7天SOFA评分,28 d内无需生命支持天数,ICU住院时长。 试验结果:两组主要终点事件无明显差异。高氧组发生SAE,肺不张和ICU获得性衰弱的比例更高。 |
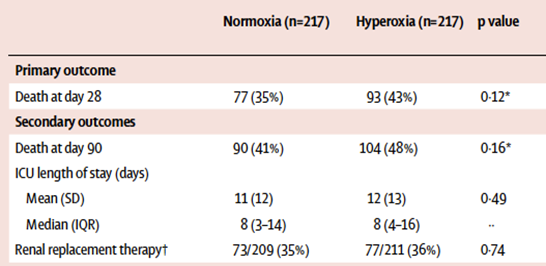

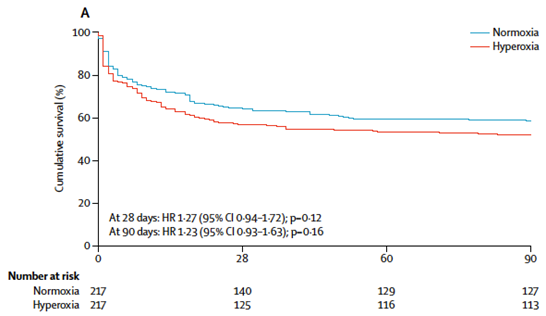
Asfar P, Schortgen F, Boisrame-Helms J, et al. Hyperoxia and hypertonic saline in patients with septic shock (HYPERS2S): a two-by-two factorial, multicentre, randomised, clinical trial[J]. Lancet Respir Med, 2017, 5(3):180-190.
ICU-ROX研究
ICU,接受有创或无创通气患者。
| 干预组:SpO2 90%以上(FiO2尽量不低于30%),PaO2 90 mmHg。 对照组:SpO2 90%~97%,PaO2 80 mmHg。 主要终点:90 d死亡率。 次要终点:ICU死亡率,院内死亡率,180 d死亡率,特定病因死亡率,生存时间,ICU时长,住院时长,无通气天数,无血管活性药天数等。 试验结果:两组无差异。 |
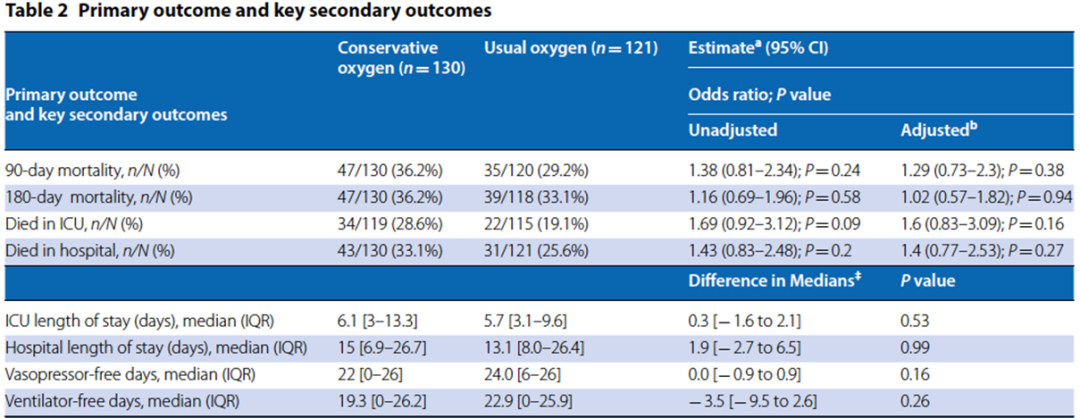
Mackle D, Bellomo R, Bailey M, et al. Conservative Oxygen Therapy during Mechanical Ventilation in the ICU[J]. N Engl J Med, 2020, 382(11):989-998.
LOCO2 研究
ARDS患者
| 干预组:PaO2 90~105 mmHg,SpO2≥96% (持续7 d)。 对照组:PaO2 55~70 mmHg,SpO2 88%~92% (持续7 d)。 主要终点:28 d死亡率。 试验结果:28 d死亡率无明显差异。 纳入205/850因安全问题(90 d病死率低氧组更高)以及试验结果不符合预期而停止。 |



Barrot L, Asfar P, Mauny F, et al. Liberal or Conservative Oxygen Therapy for Acute Respiratory Distress Syndrome[J]. N Engl J Med, 2020,382(11):999-1008.
AECOPD患者治疗重点之一是缓解疲劳的呼吸肌,推荐无创通气。但给氧需要谨慎,因为大量给氧会造成不良后果。氧气的使用会导致二氧化碳分压上升,出现二氧化碳麻醉。很长时间内,这种作用的机制被认为是COPD患者长期高碳酸状态导致颈动脉体外周化学感受器敏感度降低。这种情况下,呼吸驱动由低氧血症触发,给氧则会减少这一驱动,这就会导致分钟通气量减少和持续的高碳酸。
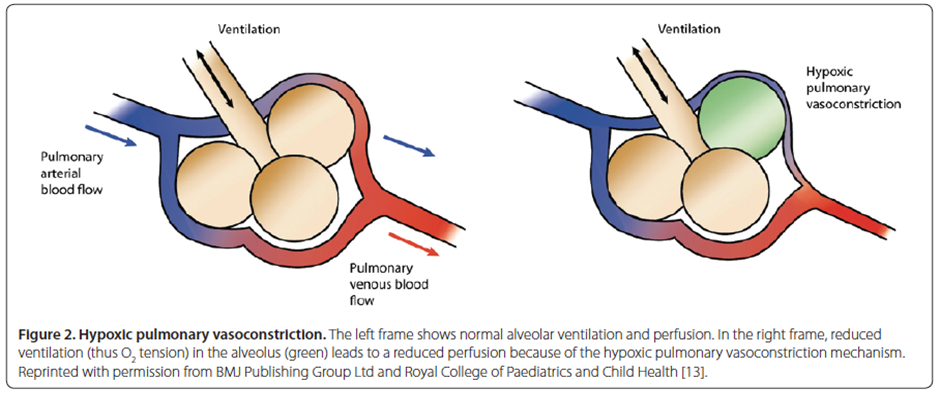
依据试验结果,这一机制只是高碳酸的原因之一,绝大多数高碳酸是因为V/Q比值改变。氧疗抑制了低氧性血管收缩,这对保持V/Q比值很重要,导致通气不太好的肺泡灌注和肺泡死腔增加。此外还有霍尔登效应(去氧Hb则容易与CO2结合,在肺部经过氧合,O2与Hb结合促使CO2释放)。AECOPD时存在高碳酸血症,Hb进一步结合CO2的能力降低。正常情况下CO2在肺部释放并被呼出,但这些患者呼吸努力已经最大,CO2难以被释放和呼出。吸氧导致Hb结合CO2减少,已结合的CO2释放增加,加剧高碳酸血症。
Abdo WF, Heunks LM. Oxygen-induced hypercapnia in COPD: myths and facts[J]. Crit Care, 2012,16(5):323

|
干预组:面罩给氧8~10 L/min。 对照组:鼻导管给氧维持SpO2 88%~92%。 主要终点:院前死亡率,院内死亡率。 试验结果:对照组死亡率更低 。 结论:推荐AECOPD患者吸氧维持SpO2 88%~92%(GOLD推荐范围)。 |
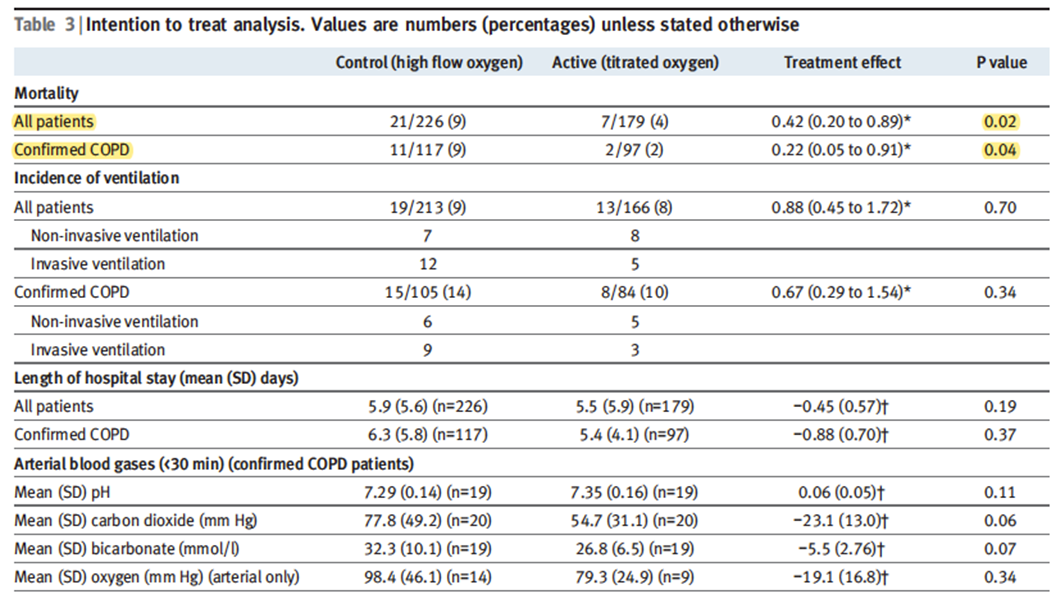
Austin MA, Wills KE, Blizzard L. Effect of high flow oxygen on mortality in chronic obstructive pulmonary disease patients in prehospital setting: randomised controlled trial[J]. BMJ, 2010, 341(341):c5462.
尽管这些例子显示给氧要慎重,但凡事均有两面。 CO中毒的情况下,必须克服CO比O2强200倍的Hb亲和力,才能维持O2输送,避免组织缺氧。因为CO和O2竞争Hb,所以治疗策略是增加O2的张力使竞争平衡倾向O2一方。 呼吸空气的情况下碳氧血红蛋白半衰期为320 min,吸氧后降低至74 min。予以20 min,2.5ATM的高压氧后,半衰期进一步降低。但转运患者去高压氧舱是比较麻烦的,目前没有共识,仅作为选择之一。 Rose JJ, Wang L, Xu Q, et al. Carbon Monoxide Poisoning: Pathogenesis, Management, and Future Directions of Therapy[J]. Am J Respir Crit Care Med, 2017, 195(5):596-606.
除了CO中毒,心搏骤停的患者也应予以纯氧以促进自主循环恢复。 但在复苏成功后,推荐降低氧分压至生理范围以避免活性氧对细胞的损伤。 一个关于氧气的问题是否存在量-效关系? 在一些临床操作如吸痰和气管插管前,我们常短时间予以高氧,这样会使肺泡功能残气脱氮,建立氧储备来延长缺氧耐受时间以避免低氧。 目前,这种短时间的高氧对患者预后是否有负面作用仍不得而知,但从另一方面讲,其可以抵消低氧带来的损伤。

急诊机械通气转入ICU后氧正常的患者(转入ICU前中位用氧时间为5.5 h)
| 组1:急诊PaO2 <60 mmHg。 组2:急诊PaO2 60~120 mmHg。 组3:急诊PaO2 >120 mmHg。 主要终点:院内死亡率。 结果:PaO2 >120 mmHg组死亡率明显高于另外两组。 虽然这是一项回顾性研究,但结果提示即使几个小时的高氧也会对预后造成负面影响。 |
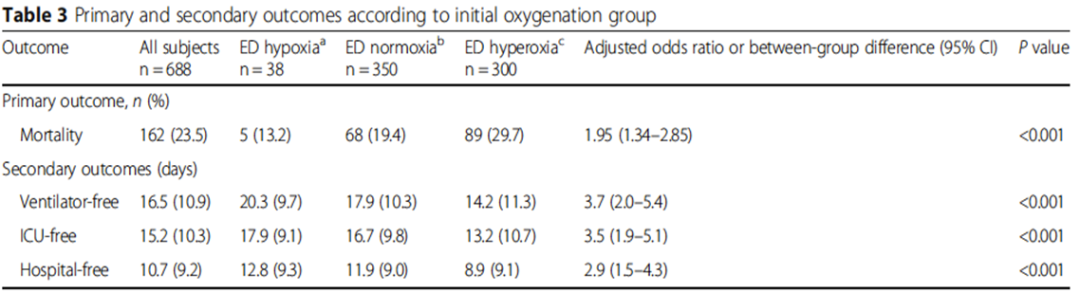
Page D, Ablordeppey E, Wessman BT, et al. Emergency department hyperoxia is associated with increased mortality in mechanically ventilated patients: a cohort study[J]. Crit Care, 2018, 22(1):9.
HOT-ICU
ICU患者,开放吸氧10 L/min或密闭吸氧FiO2 50%以上| 组1:PaO2 90 mmHg。 组2:PaO2 60 mmHg。 主要终点:90 d全因死亡率。 次要观察结果(无支持下存活,出院后存活)以及SAE。 试验结果:两组无差异。 |
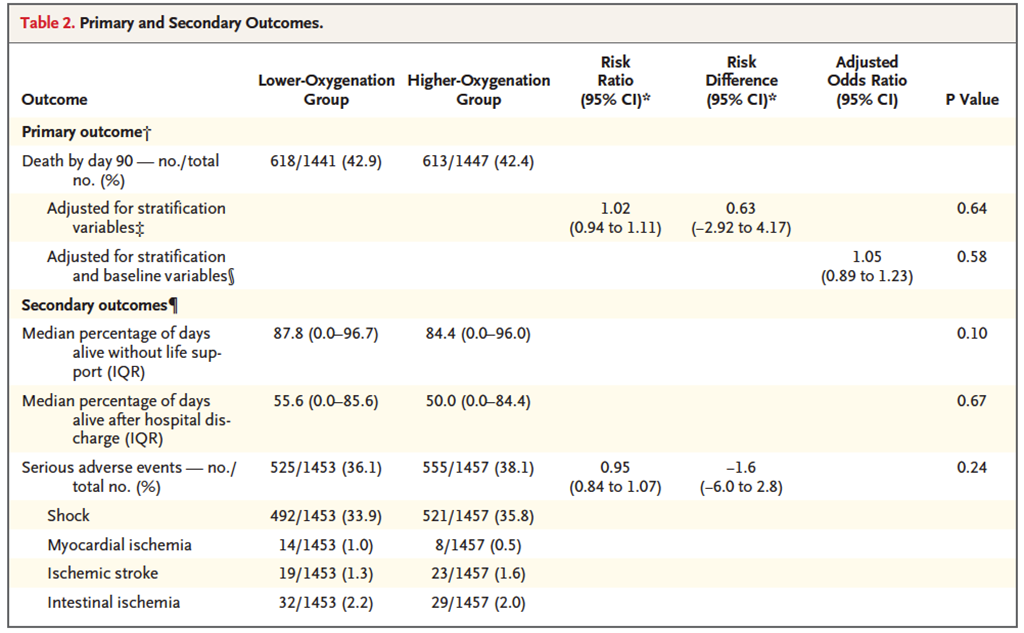
Schjørring OL, Klitgaard TL, Perner A, et al. Lower or Higher Oxygenation Targets for Acute Hypoxemic Respiratory Failure[J]. N Engl J Med, 2021, 384(14):1301-1311.

尽管对最优给氧值的探索还在继续,未来有可能阐明用氧的量-效关系,目标性给氧是很重要的,因为高氧会带来损伤,至少不会获益。因为长期的对低氧增加病死率的印象,所以目标性给氧的应用可能会比较困难。另一方面,一种循序渐进联合跨专业培训的方式已经被证明是可行的。